Nature实锤!「肥胖记忆」才是复胖元凶!99%的产品都忽视了这一核心痛点
为什么消费者在减重道路上反复失败,真的只是意志力不足吗?
前沿科学给出了一个颠覆性的答案:“肥胖记忆”(Obesity Memory)。
它告诉我们,减重失败的根源并非毅力,而是一种深刻的生理烙印——即使体重成功减轻,身体的肠道、免疫系统乃至大脑,依然“记得”着曾经的肥胖状态,并通过4大核心机制,让身体悄悄复胖。
正确理解肥胖记忆,才能精准切入体重管理市场核心痛点——维持体重、防止反弹的关键,也为抓住当前市场的空白和机遇提供了科学指引。
一、核心解读:什么是肥胖记忆?
从学术角度上讲,肥胖记忆是指:在体重显著减轻后,脂肪组织(尤其是脂肪细胞、脂肪祖细胞和内皮细胞)仍通过表观遗传修饰(如DNA甲基化、组蛋白修饰等)保留的、持久存在的肥胖时期分子特征。这种记忆使细胞在再次暴露于致肥环境时,更容易激活与炎症、代谢失调相关的基因表达,从而导致体重反弹。
多项前沿研究表明,肥胖记忆并非简单的生活习惯问题,而是具有深刻的生物学基础,主要通过以下几个关键机制发挥作用:

1.肠道菌群失衡
肠道菌群的失衡是构成肥胖记忆的核心环节之一。
 图源:FDL数食有料
图源:FDL数食有料
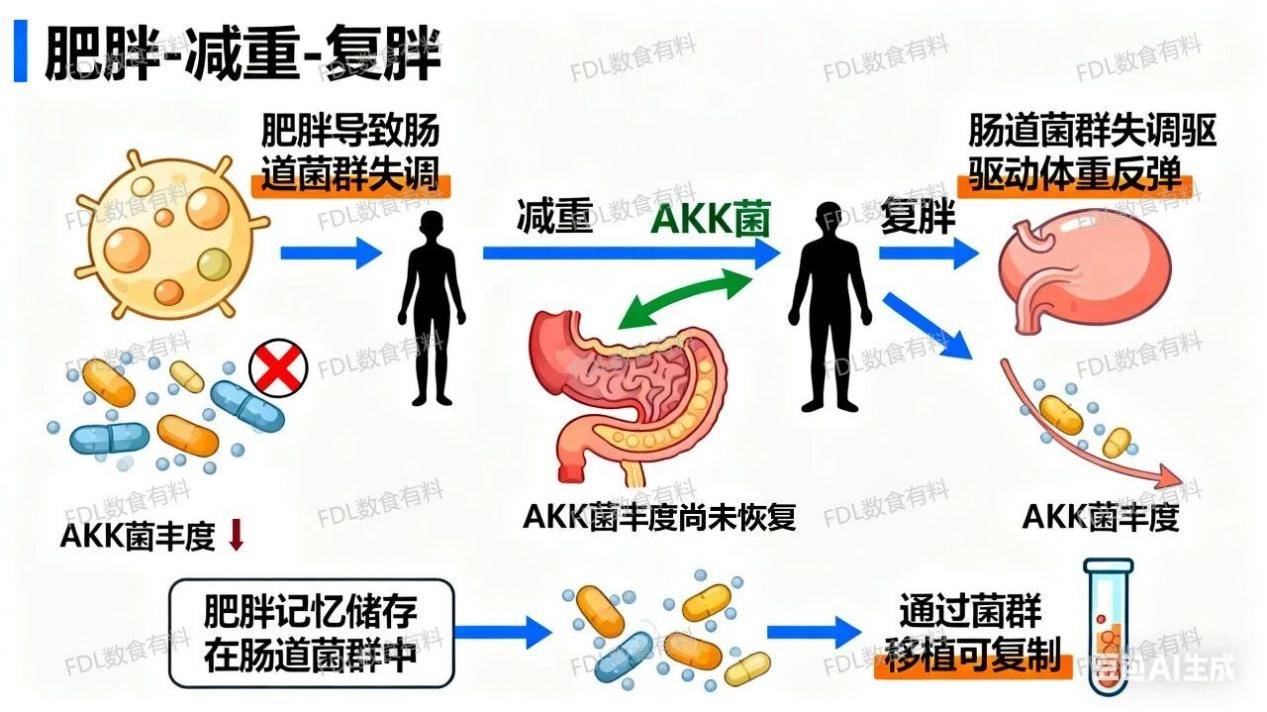
一项发表于《Nature》的研究表明[1][2],肥胖会引起肠道菌群的显著失调,并且这种失调状态在成功减重后并不会完全恢复正常。 例如,有益菌AKK的丰度仍维持在较低水平。这种持续的菌群失衡构成了体重快速反弹的生物学基础。
关键的菌群移植实验进一步证实:将减重后复胖小鼠的肠道菌群移植给无菌小鼠,后者也表现出同样的快速复胖倾向。这一结果表明,导致减肥后易复胖的“肥胖记忆”就储存在失衡的肠道菌群中,其驱动效应可通过菌群转移。
2. 免疫-神经轴的炎症记忆
 图源:《Nature》
图源:《Nature》
肥胖本身是一种慢性低度炎症性疾病,这种炎症状态会在免疫系统和神经系统中留下持久的记忆。
一项发表于《Nature》期刊的研究揭示,肥胖会驱动脂肪组织中促炎性免疫细胞(如巨噬细胞)的大量浸润与活化,并显著提升炎症因子(如TNF-α、IL-6)的表达水平,造成全身性的慢性炎症。而身体会对肥胖形成“免疫记忆”,减肥后促炎巨噬细胞仍潜伏在脂肪组织中,一旦遇到刺激就容易重新激活炎症,导致体重反弹。
进一步,持续的神经炎症会对下丘脑(控制食欲、饱腹感和能量消耗的核心中枢)的神经元造成损害,并干扰关键激素信号的传导。
比如,这种炎症会干扰瘦素和胰岛素等关键激素的信号传导,损害其受体及下游通路,引发中枢性瘦素抵抗与胰岛素抵抗[5],从而削弱大脑对能量状态的感知与调控能力。
此外,炎症反应甚至可以直接导致调节能量平衡的关键神经元(如POMC神经元)损伤或死亡,从根本上破坏身体的能量稳态调节网络[6]。
3.脂肪组织的表观遗传学改变
表观遗传学是指在不改变DNA序列的前提下,通过化学修饰调控基因的活性状态,并且这种状态能在细胞分裂时稳定地遗传给子代细胞。
 图源:《Nature》
图源:《Nature》
一项发表于《Nature》,由Hinte团队(2024)领导的研究,揭示了:脂肪细胞会通过表观遗传变化保留肥胖记忆,导致即使减肥后仍容易体重反弹。[3]
研究人员通过对比人类和老鼠在减肥前后的脂肪组织样本,发现其脂肪细胞的基因表达和表观遗传标记(如染色质可及性和组蛋白修饰)在减肥后仍保留肥胖时期的特征。同时,减肥后的小鼠在重新接触高脂饮食时,会比从未肥胖的小鼠体重反弹得更快。
4.线粒体功能障碍
 图源:《Nature-metabolism》
图源:《Nature-metabolism》
最后,肥胖记忆还体现在脂肪细胞自身的代谢功能缺陷上。
一项发表于《Nature Metabolism》(自然-代谢)的研究揭示了导致肥胖难以逆转的另一个关键机制。该研究指出,核心问题在于脂肪细胞自身的代谢功能受损,具体表现为细胞内线粒体的功能障碍与碎片化,导致身体难以通过ATP代谢和产热来消耗多余能量。
进一步的分子研究确认,这一系列功能障碍的根源在于RalA基因。在肥胖状态下,RalA基因被过度激活,从而驱动线粒体发生过度分裂,最终导致其碎片化和功能失常[4]。
 脂肪组织 图源:KateStudio/Shutterstock.com
脂肪组织 图源:KateStudio/Shutterstock.com
总结而言,“肥胖记忆”是一个复杂且多维度的生物学现象。它并非单一因素导致,而是由肠道菌群失衡、慢性神经免疫炎症、脂肪细胞表观遗传改变以及线粒体功能障碍这四大机制共同作用、相互影响的结果。
这些深刻的生物学印记解释了为何减肥后的体重维持如此困难,也强调了长期、科学的体重管理策略远比短期的快速减重更为重要。
二、「传统体重管理」模式VS「对抗肥胖记忆」新模式
在深入理解上述四大肥胖记忆的底层机制之后,可以清晰地认识到,为何传统的体重管理模式往往只能治标而难以治本。

通过对比不难发现:传统模式的核心是帮助用户对抗身体,通过节食和运动强行制造热量缺口。
而未来的机遇在于,开发出能帮助用户修复身体的科学配方,从根源上消除或改善肥胖记忆带来的生理障碍。
这才是真正切入防反弹这一核心痛点,打造高壁垒产品的差异化思路。
三、创新方向:对抗肥胖记忆的功能性成分清单
针对肥胖记忆的四大核心机制,FDL数食有料详细列举了一系列前沿的功能性成分,并拆解其核心机制。
l 针对肠道菌群记忆——微生态重塑
为实现肠道微生态的重塑,可以运用AKK菌、尿石素A以及三丁酸甘油酯等成分,通过调节免疫、强化肠道屏障、改善菌群环境等机制,对抗并改善由菌群失衡导致的肥胖记忆。
- AKK菌(嗜黏蛋白阿克曼氏菌):AKK菌主要通过其细胞膜上保留的活性成分(如外膜蛋白Amuc_1100和特定磷脂)与宿主免疫系统相互作用,调节免疫反应、减轻炎症并增强肠道屏障功能,从而为有益菌的生长创造有利条件
- 尿石素A:属后生元,由肠道菌群代谢产生,可激活线粒体自噬,强化肠道屏障(上调紧密连接蛋白),调节肠道炎症
- 三丁酸甘油酯:属后生元,在肠道内分解为丁酸,丁酸作为肠道细胞的主要能源,修复肠道屏障。创造酸性环境,抑制有害菌生长,促进有益菌增殖
l 针对免疫-神经轴的炎症记忆——抑制炎症、调节免疫记忆和保护神经元
为了对抗免疫-神经轴的炎症记忆,可以通过补充PQQ(吡咯并喹啉醌)、羟基酪醇、蓝莓花色苷/黑枸杞/黑桑葚、NMN、三丁酸甘油酯、人参粉、亚精胺、尿石素A、麦角硫因以及白藜芦醇与EGCG等多种活性成分,通过穿越血脑屏障、抑制炎症因子、清除自由基和保护神经元等维度,实现对炎症的有效抑制与调节。
- PQQ(吡咯并喹啉醌):通过刺激神经生长因子(NGF)的合成、保护神经元免受氧化损伤以及促进脑细胞中新线粒体的生成来支持大脑神经健康
- 羟基酪醇/橄榄果粉:作为小分子量的强抗氧化剂,可穿过血脑屏障,抑制小胶质细胞活化,减少促炎细胞因子产生,对抗神经炎症
- 蓝莓花色苷 /黑枸杞 /黑桑葚:花色苷(或称花青素)及其代谢产物已被证实可以穿过血脑屏障。通过强大的抗氧化作用清除大脑自由基,下调炎症信号通路,保护神经元
- NMN(烟酰胺单核苷酸):
- 提升细胞内NAD⁺水平,改善线粒体功能,激活SIRT1蛋白,抑制NF-κB炎症通路,抑制神经炎症
- 三丁酸甘油酯:作为丁酸前体,丁酸穿过血脑屏障后作为组蛋白去乙酰化酶(HDAC)抑制剂,调节小胶质细胞功能,发挥抗炎作用
- 人参粉:其人参皂苷成分抑制小胶质细胞过度活化,减少炎症介质(如NO和TNF-α)的释放
- 亚精胺、尿石素A、麦角硫因:亚精胺诱导细胞自噬,尿石素A诱导线粒体自噬,两者可减少炎症触发因素;麦角硫因具有超强抗氧化能力,清除自由基,保护神经元免受氧化损伤和炎症反应
- 白藜芦醇、表没食子儿茶素没食子酸酯(EGCG):EGCG与白藜芦醇联合使用时,可下调肥胖者脂肪组织中与炎症、免疫防御和氧化应激相关的基因表达通路
l 针对表观遗传记忆——直接或间接影响表观遗传修饰酶
表观遗传调控主要通过两大核心机制来决定基因的表达状态:一是DNA甲基化,二是组蛋白修饰(如乙酰化/去乙酰化)及其导致的染色质可及性改变。
要改善由这些表观遗传改变所导致的体重反弹易感性,就需要寻找能够直接或间接调节关键表观遗传修饰酶(如组蛋白去乙酰化酶HDACs、组蛋白乙酰转移酶HATs、DNA甲基转移酶DNMTs等)活性的生物活性成分。
相关的代表性成分有:三丁酸甘油酯、AKG(α-酮戊二酸)、NMN(烟酰胺单核苷酸)。
- 三丁酸甘油酯:经肠道代谢为丁酸,丁酸是研究最为透彻的组蛋白去乙酰化酶(HDAC)抑制剂之一,可逆转脂肪组织表观遗传记忆,和减少炎症因子释放
- AKG(α-酮戊二酸):AKG通过表观遗传调控(DNA去甲基化)、AMPK激活、OXGR1/PHD3信号通路等多机制促进棕色脂肪生成和产热,改善肥胖及相关代谢紊乱
- NMN(烟酰胺单核苷酸):NMN通过提升细胞内NAD⁺水平,激活SIRT1(第三类组蛋白去乙酰化酶),有效逆转肥胖状态下不利的组蛋白乙酰化模式
l 针对线粒体崩坏——能量工厂的修复与激活
针对线粒体功能障碍这一问题,可以通过补充PQQ(吡咯并喹啉醌)、NMN(烟酰胺单核苷酸)、尿石素A、亚精胺、AKG(α-酮戊二酸)以及葫芦巴碱等多种功能性成分,从增加数量、修复功能、清除损伤和优化产能等多个维度实现对线粒体的修复与激活。
- PQQ(吡咯并喹啉醌):激活PGC-1α信号通路,促进线粒体生成(直接增加线粒体数量)
- NMN (烟酰胺单核苷酸):作为NAD⁺的关键前体,通过提升细胞内NAD⁺水平来改善线粒体电子传递链功能并增强ATP生成,从而修复受损的线粒体功能
- 尿石素A:激活线粒体自噬,促进受损线粒体的降解与清除,以维持线粒体网络的质量和稳态
- 亚精胺:激活细胞自噬,促进受损线粒体的降解与清除
- AKG(α-酮戊二酸):作为三羧酸循环的核心代谢物,直接参与并优化线粒体能量生成过程,提升氧化磷酸化效率与ATP产量
- 葫芦巴碱:作为NAD⁺的前体,高效提升NAD⁺水平,从而激活线粒体功能,促进能量代谢
四、市场洞察:为何现在是最佳时机?
深刻理解肥胖记忆的生物学机制后,可以发现,一个基于前沿科学、直击消费者核心痛点的巨大市场机遇正在浮现。
当前,中国的肥胖问题日益严峻——34.3%成年人超重,16.4%成年人肥胖,儿童青少年超重肥胖率19.0%[7]。在中国庞大的人口基数加成下,体重管理成为了持续且刚性的需求。
同时,与肥胖相关的慢性病,如2型糖尿病、心血管疾病等发病率持续攀升,体重管理已从美观需求升级为国民健康刚需。
然而,传统体重管理市场已成红海,内卷严重且增长乏力。
当前市场主要由代餐、运动营养品和各类阻断剂主导。这些产品虽然在短期内可能有效,但同质化现象极为严重,品牌陷入价格战和营销战泥潭。消费者在经历了快减快反的循环后,对传统产品的信任度和复购率逐渐下降,行业亟需颠覆性创新打破增长瓶颈。
 图源:freepik
图源:freepik
而随着健康知识普及,消费者开始关注新陈代谢、肠道健康、棕色脂肪等深层机制。肥胖记忆概念虽前沿,但其背后的科学逻辑(如肠道菌群、炎症等)与消费者日益增长的认知需求高度契合,更易获得市场认同。
此外,此外,经历反复失败的消费者更深刻认知到:体重反弹是比减重更严峻的挑战。因此,一种长期、可持续的体重维持方案,更能击中消费者的痛点需求。
在此机遇下,开发基于"肥胖记忆"的产品,正是构筑科学壁垒与差异化叙事的关键。当传统品牌还在宣传"管住嘴、迈开腿"时,"对抗肥胖记忆"的前沿科学叙事能快速实现差异化定位,塑造高端专业形象,摆脱同质化竞争!
——————————————————————————————————————
抢占市场先机,打造您的下一款明星产品,现在正是最佳时机!
立刻联系我们,获取前沿原料市场报告、最新报价、前沿配方、应用资讯。我们的专家团队将为您提供一对一的咨询服务,从科学到商业,全方位助您开启成功之路!
数食有料 foodingredient
入驻媒体平台:36氪\界面\钛媒体\今日头条\
百家号\新浪微博\搜狐\网易\知乎\小红书等
文章转载|合作请添加微信:foodatalink789
联系邮箱:fooddatalink@beautydata.ai
参考文献
[1] Thaiss Christoph A, et al. (2016). Persistent microbiome alterations modulate the rate of post-dieting weight regain.
[2] 《Nature子刊背书! AKK菌有望攻克减肥反弹死循环》,FDL数食有料
[3] Hinte, L.C., Castellano-Castillo, D., Ghosh, A. et al. Adipose tissue retains an epigenetic memory of obesity after weight loss. Nature 636, 457–465 (2024).
[4] Xia, W., Veeragandham, P., Cao, Y., Xu, Y., Rhyne, T. E., Qian, J., ... Saltiel, A. R. (2024). Obesity causes mitochondrial fragmentation and dysfunction in white adipocytes due to RalA activation. *Nature Metabolism*. https://doi.org/10.1038/s42255-024-00978-0
[5] Heiss, C. N., Mannerås-Holm, L., Lee, Y. S., Serrano-Lobo, J., Håkansson Gladh, A., Seeley, R. J., Drucker, D. J., Bäckhed, F., & Olofsson, L. E. (2021). The gut microbiota regulates hypothalamic inflammation and leptin sensitivity in Western diet-fed mice via a GLP-1R-dependent mechanism. Cell Reports, 35(8), 109163.
[6] Front. Neurosci.全面综述:环境—肥胖—神经系统疾病的复杂关系
[7] 《中国居民营养与慢性病状况报告(2020年)》
